CÁNCER DE TIROIDES DIFERENCIADO (Differentiated Thyroid Cancer, DTC)
Papilar (Papillary Thyroid Cancer, PTC) - 89%. Se caracteriza por la presencia de alteraciones genéticas como BRAF V600E (60%), RAS (13%), fusión RET (6.3%), NTRK (2.3%), fusion ALK (0.8%).
Folicular (Follicular Thyroid Cancer, FTC) - 5%.
Oncocítico (Oncocytic Cell Carcinoma, OCA) - 2%
La prevalencia es mayor en mujeres. La mayoría de los casos del DTC tienen buen pronóstico y en principio son manejados por endocrinología y cirugía de cabeza y cuello. La estratificación del riesgo se basa en los hallazgos patológicos de la tiroidectomía total y en base a ese riesgo se define el uso de yodo radiactivo (RAI), supresión de la TSH y posterior vigilancia basada en la respuesta obtenida. Pronóstico: SG a 5años: 95%, SG a10 años: 86% (42% si hay metastasis), SG a 15 años: 81% (33% si hay metástasis).
Características de alto riesgo:
Invasión macroscópica del tumor (gross ETE)
Resección incompleta del tumor
Metástasis a distancia (mas allá del cuello)
Cáncer folicular de tiroides con invasión vascular extensa (>4 foci)
Ganglios ≥3cm (N1)
Pese al buen pronóstico, un 10% de los DTC progresará a un cáncer de tiroides avanzado, de los cuales 2/3 (67%) serán refractarios a yodo (RAIR) y requerirán terapias adicionales.
CÁRCINOMA DE TIROIDES DE ALTO GRADO DERIVADO DE CELULAS FOLICULARES -NO ANAPLÁSICO.
Prevalencia 1-10% de todos los cánceres de tiroides (<5% en USA, <1% en Japón, >5% en América Latina e Italia, variabilidad por posibles diferencias étnicas y deficiencia de yodo). La prevalencia es similar en hombres y mujeres. Su presentación ocurre en 5ta y 6ta década del vida. 50% no captan yodo de inicio, tienen peor pronóstico que los DTC. Hay dos grupos:
Carcinoma de tiroides diferenciado de alto grado (Differentiated High Grade Thyroid Cancer, DHGTC): se caracteriza por ser bien diferenciado (tienen componente de PTC, FTC or OCA), no tiene características anaplásicas, mitosis ≥5/2 mm (10 HPFs) o necrosis tumoral, sin rasgos anaplásicos. Al diagnóstico entre el 12-73% tienen metastasis ganglionares y 6-40% metástasis a distancia.
Carcinoma de tiroides pobremente diferenciado (Poorly Differentiated Thyroid Cancer, PDTC): se caracteriza por ≥3/2 mm (10 HPFs) o necrosis o núcleo complejo, sin rasgos anaplásicos. El patrón de crecimiento es mas sólido/insular. Al diagnóstico entre 4.5-50% tienen metástasis ganglionares y 8-27% tienen metástasis a distancia. la SG a 5 años es de 50% (rango 47-89%), SG a 10 años es de 34%, SG a 15 años es 0%.
Evaluación inicial:
Ante una histología de alto grado, se debe:
Evaluar comorbilidades (diabetes, hipertensión arterial, enfermedad renal crónica), ante la posibilidad de una terapia sistémica.
Revisar patología por un experto para evitar que se escape un caso de carcinoma anaplásico
Descartar metástasis (idealmente con PET-CT): los sitios más frecuentes de metástasis son los ganglios cervicales, pulmones, hígado y óseo. Pero puede haber metástasis en cualquier parte del cuerpo. Evaluar la piel por frecuentes metástasis cutáneas y sistema nervioso central.
Monitorear la tiroglobulina (Tg) en especial, después del tratamiento para detectar remanente de tejido tiroideo o recidiva tumoral. La prevalencia de anticuerpos anti-tiroglobulina (TgAb) en cáncer de tiroides es del 20-30%, lo cual puede generar interferencia en la medición de Tg en laboratorio, provocando un resultado falsamente bajo o indetectable.
Estudios moleculares para identificación de mutaciones "driver", segun disponibilidad se puede usar técnicas como IHC para BRAF, NGS en tejido o biopsia líquida en sangre periférica (menos sensible).
Criterios de refractariedad a yodo radioactivo (RAIR)
Aún hay variabilidad de criterios de refractariedad en la literatura.
Metástasis que no concentran RAI de inicio
Perdieron a avidez después de haber sido tratados con RAI.
Población mixta donde unas lesiones captan RAI y otras no captan.
Progresión metastásica significativa después de haber recibido tratamiento con RAI dentro de 6-12m.
Alta avidez en de lesiones en PET-CT (FDG)
Manejo:
Monitoreo activo: si tiene baja carga tumoral y/o la progresión es muy lenta.
Oligometástasis: se puede realizar cirugía si es factible, terapias locales como radioterapia, ablación térmica o embolización en metástasis hepáticas.
Lesiones óseas :se benefician de bifosfonatos o inhibidores de RANK-Ligandos.
Tratamiento sistémico es indicado cuando hay tumor con localización amenazante, enfermedad pulmonar con patrón miliar sintomático, carga tumoral significativa.
Dabrafenib + trametinib (Inhibidores de BRAF y MEK): terapia dirigida en casos de mutación BRAF V600E. Aprobado para cancer anaplásico de tiroides en el cual tiene respuestas muy rápidas (días) y profundas, ORR 69%, OS 1 año: 80%. En cancer diferenciado de tiroides la respuesta es menos profunda, incluso no hay gran diferencia en usar dabrafienib solo vs la combinacion dabrafenib + trametinib (ORR 50% vs 54% y PFS 11.4 vs 15.1 meses), esto permite flexibilidad para el tratamiento especialmente en pacientes geriátricos. Un efecto adverso importante es la fiebre, en Japón está aprobada la combinación de encorafenib más binimetinib que produce menos fiebre.
Sorafenib vs placebo (ITK multi kinasa): SLP 10.8m vs 5.8 m, principal efecto adverso es el sindrome mano-pie
Lenvatinib vs placebo (ITK multi kinasa): SLP 18.3m vs 3.6m en primera línea. Respuesta parcial: 63% y respuesta completa: 1.5%. En segunda línea PFS de 15 meses. Dosis de inicio es de 24 mg día. Un estudio que comparó 24 mg vs 18 mg de inicio mostró que había mayor respuesta tumoral con la dosis de 24 mg, sin diferencia significativa en reacciones adversas severas PMID: 34664662, 2022, J Clin Endocrinol Metab). Se puede usar después de terapia dirigida.
Cabozantinib- COSMIC 311 trial (ITK multi kinasa): uso en el manejo de DTC RAIR en segunda línea después de progresión a sorafenib o lenvatinib . PFS 11 m vs 1.9 meses con placebo. (Brose et al. 2021). Dosis: 60 mg/día.
Selpercatinib (Inhibidor de fusiones RET, mas frecuentes en jóvenes o con radiación previa). Aprobado por FDA para cancer de tiroides papilar, pobremente diferenciados, celular de Hurtle y Anaplasico (Wirth LJ, nejm. 2020). ORR 79%, PR 74%, duración de la respuesta de 18.4 meses. Los efectos adversos de los inhibidores de RET usualmente son manejables (Tabla 1), 30% necesitan reducción de dosis y 2% descontinuación de la terapia. Otros efectos adversos grado 1/2 son boca seca, náuseas, constipación, edema, aumento de creatinina, dolor abdominal, artralgias, hipotiroidismo, mareo, tos y rash.
Pralsetinib (Inhibidor de fusiones RET): indicación en DTC RAIR con fusión RET. ORR 89%, PR 89%, Mediana de duración de la respuesta no alcanzada.
Terapia de rediferenciación: en el momento no esta incluida en las guias de cancer de tiroides, dado que los estudios son heterogeneos, pero consiste que en aquellos pacientes en los cuales no se haya maximizado la cantidad de RAI durante su vida, se puede usar una terapia blanco por 4 semanas y si en un rastreo hay captación de RAI, se puede administrar una dosis adicional (inhibidores de BRAF), logrando reducción de 40-60% del tamaño de las lesiones. La estrategia es atractiva por la posibilidad de descontinuar la terapia sistémica de manera temporal en casos muy selectivos. Se espera nuevos estudios para definir cual será el mejor momento para su incorporación.
GENERALIDADES
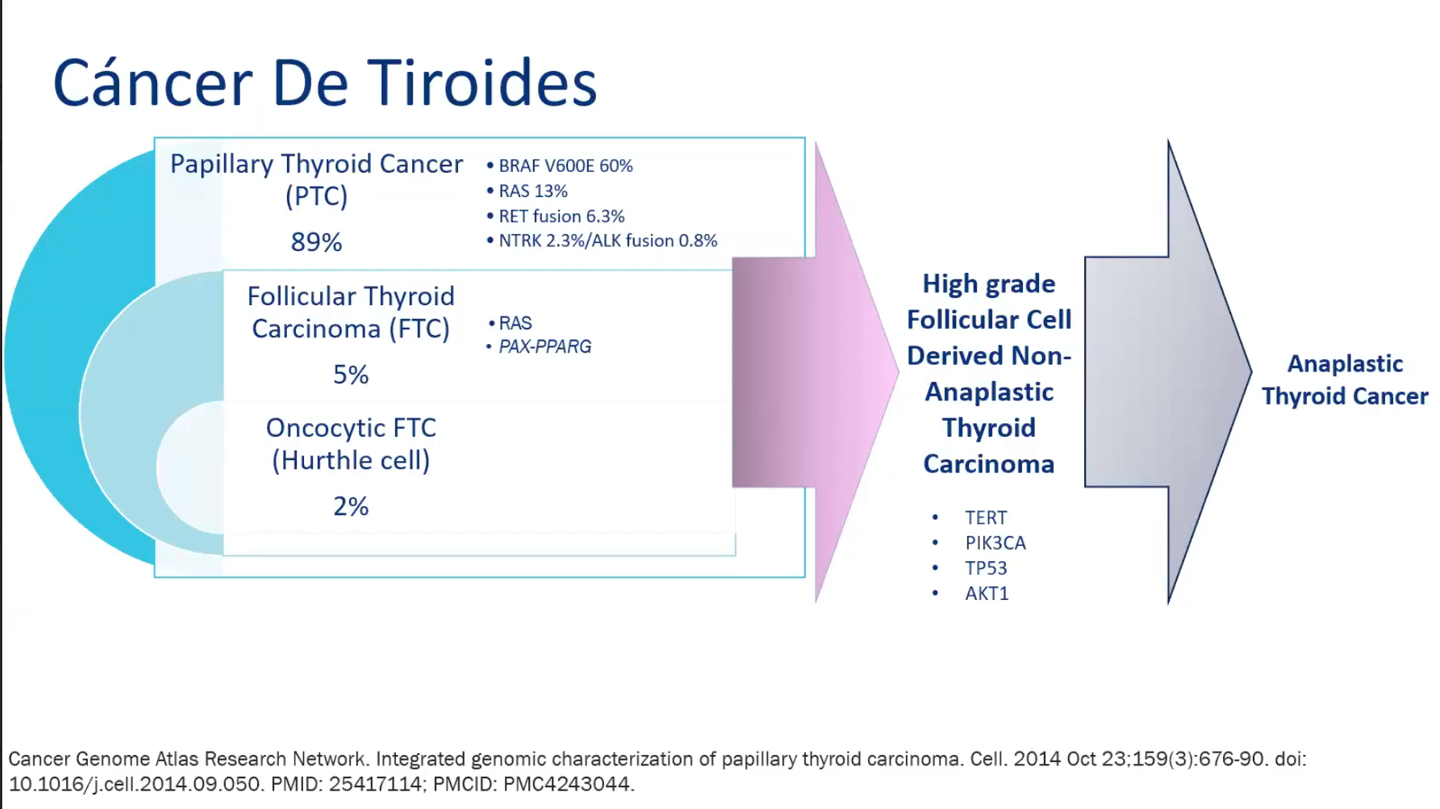
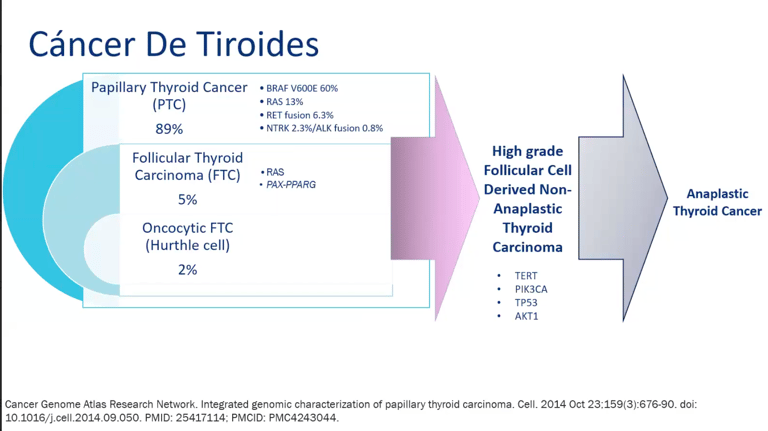
El cáncer de tiroides comprende un gran espectro, empieza como un cáncer diferenciado y de buen pronóstico, que posteriormente puede adquirir nuevas alteraciones genéticas (como TERT, TP53, AKT-1, PIK3CA) y exhibir un comportamiento menos diferenciado, el cual se ubica en un punto intermedio del espectro, denominado carcinoma de tiroides de alto grado (este grupo comprende los carcinomas diferenciados de alto grado y carcinomas pobremente diferenciados), que se correlacionan con pobre respuesta a la terapia con yodo radioactivo.
CÁNCER DE TIROIDES AVANZADO
DTC que progresan a cáncer de tiroides avanzado (<10% de los DTC), el 67% serán RAIR
Carcinoma medular de tiroides (casos metastásicos)
Carcinoma anaplásico de tiroides.
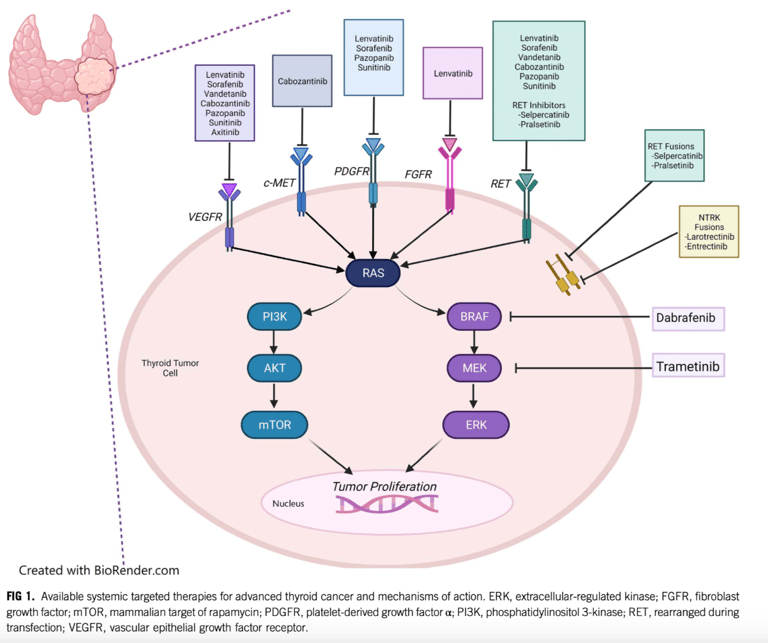
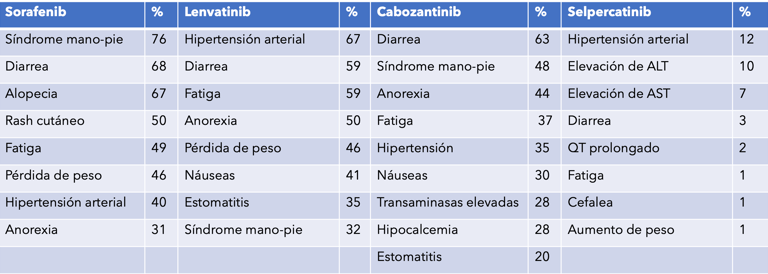
Fig 2. Mecanismo de acción de terapia sistémica.
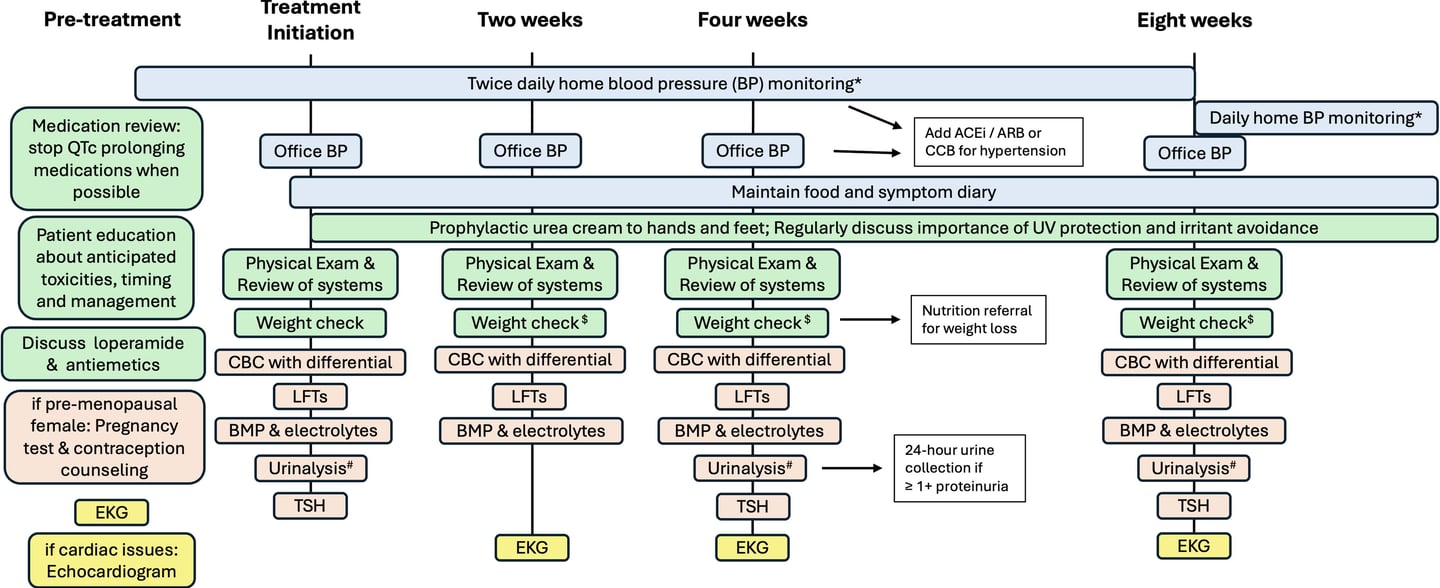
Tabla 1. Efectos adversos del tratamiento sistémico
Fig 3. Monitoreo de eventos adversos durante el tratamiento